Те, що все ізобари сходяться в одній точці (рис. 1.9), не випадковість, а закономірний-ність, що має певний фізичний зміст. Закон Гей-Люссакане заперечую воз-можности безмежного зростання температури, адже обсяг газу при зростанні температури може необмежено увеличи-тися. Проте при зниженні тим-ператури він прагне до нуля і має гра-ніцу ( V = 0), Оскільки не може бути отри-цательного.
Насправді реальні гази навіть не можуть досягти цієї межі, оскільки їх атоми і молекули, хоч і маленькі за розміром, все-таки мають певний обсяг.
Якщо в рівнянні (V -V 0) /V 0 =αΔ t,припускає-ложить, що V 0 -це обсяг газу при t 0= 0 ° C, отже, Δ t =t -t 0 =t,і прирівняти його до нуля як нижній межі обсягу, то по-лучім значення найнижчої температури за шкалою Цельсія, яку можуть мати тіла:
0 = V 0. (1 + t / 273).
1 + t / 273 = 0, t = -273° C
Отже, температура може безмежно по-вишу, але в природі існує її нижню межу - абсолютний нуль,нижче якого вона не може опускатися. Ось чому з-бари всіх газів сходяться в одній точці на осі температур, яка дорівнює -273 ° C.
Не всі в світі від-носительно; існують і абсо-лютні значення, зокрема абсолютний нуль температур.
існування абсолютного нуля темпе-ратурабуло покладено англійським вченим У. Томсоном ( Кельвіном) В основу побудувати-ення абсолютної шкали температур, Ко-торая не залежить від властивостей метричного тіла і тому може вважатися ідеальною. Матеріал з сайту

Вільям Томсон (Лорд Кельвін) (1824 - 1907). Англійський фізик, один з ос-нователей термодинаміки і молекулярно-кінетичної теорії, теорії термо-електричних явищ, основ елект-ромагнітних коливань. Сформулювати-вал другий закон термодинаміки, ввів абсолютну шкалу температур (шкала Кельвіна), відкрив термодинамічний ефект, вивів формулу періоду соб-дарських електромагнітних коливань в коливальному контурі, здійснив розрахунки розмірів молекул і т. Д. За видатні наукові досягненняпо-лучіл титул лорда Кельвіна.
Точкою відліку шкали є абсолютний нуль температури, Точне значення кото-рого дорівнює -273,15 ° С. Одиницею изме ренію обрана величина, яка в СІ на-ни опиняються Кельвіном(К); вона за розміром дорівнює градусу Цельсія(° С): 1 К = 1 ° С. По-цьому між абсолютною температурою Ті температурою за шкалою Цельсія tсуще-ствует просте співвідношення (рис. 1.10):
T =t + 273.
поняття абсолютної температуриширо-ко використовують в термодинаміки і молекулами-лярной фізики, оскільки воно має глиб-кий фізичний зміст і спрощує запис багатьох рівнянь.
На цій сторінці матеріал за темами:
Термодинамічна шкала температур абсолютний нуль конспект
Лекція абсолютна шкала температур
Термоелектричним явищ і молекулярної фізики
-
Температура є кількісною мірою «нагретости» тіла. Поняття температури займає особливе місце в ряду фізичних величин, Що визначають стан системи. Температура не тільки характеризує стан теплової рівноваги даного тіла. Вона є також тим параметром, який приймає однакове значення для будь-яких двох або більшого числа тіл, що знаходяться в тепловій рівновазі один з одним, тобто характеризує теплове рівновагу системи тіл. Це означає, що якщо два або кілька тіл, що мають різні температури, привести в контакт, то в результаті взаємодії між молекулами ці тіла візьмуть однакове значення температури.
Молекулярно-кінетична теорія дозволяє з'ясувати фізичний зміст температури. Порівнюючи вирази (2.4) і (2.7), бачимо, що вони збігаються, якщо покласти
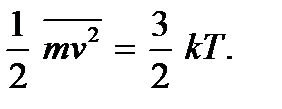 (2.9)
(2.9)Ці співвідношення називають другими основними рівняннями молекулярно-кінетичної теорії газів. Вони показують, що абсолютна температурає величина, яка визначає середню кінетичну енергію поступального руху молекул; вона є мірою енергії поступального руху молекул, а тим самим і інтенсивності теплового руху молекул. У цьому полягає молекулярно-кінетичний сенс абсолютної температури. Як бачимо, процес нагрівання тіла безпосередньо пов'язаний зі збільшенням середньої кінетичної енергії частинок тіла. З (2.9) видно, що абсолютна температура - величина позитивна:
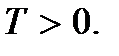 значення
значення 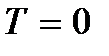 називається абсолютним нулем температури. Згідно (2.8) при абсолютному нулі повинно повністю припинятися поступальний рух частинок (
називається абсолютним нулем температури. Згідно (2.8) при абсолютному нулі повинно повністю припинятися поступальний рух частинок ( 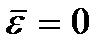 ). Слід, однак, відзначити, що при низьких температурах газ переходить в конденсована стан. Отже, втрачають сенс і всі висновки, зроблені на основі кінетичної теорії газів. І при абсолютному нулі температури рух не зникає. Рух електронів в атомах, рух вільних електронів в металах повністю зберігаються і при температурі абсолютного нуля. Крім того, навіть при абсолютному нулі зберігається деякий коливальний рух атомів всередині молекул і атомів у вузлах кристалічної решітки. Існування цих коливань пов'язано з наявністю нульової енергії у квантового гармонічного осцилятора (
). Слід, однак, відзначити, що при низьких температурах газ переходить в конденсована стан. Отже, втрачають сенс і всі висновки, зроблені на основі кінетичної теорії газів. І при абсолютному нулі температури рух не зникає. Рух електронів в атомах, рух вільних електронів в металах повністю зберігаються і при температурі абсолютного нуля. Крім того, навіть при абсолютному нулі зберігається деякий коливальний рух атомів всередині молекул і атомів у вузлах кристалічної решітки. Існування цих коливань пов'язано з наявністю нульової енергії у квантового гармонічного осцилятора ( 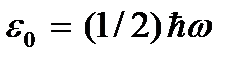 ), В якості якого можна розглядати зазначені вище коливання атомів. Ця енергія не залежить від температури, а значить, не звертається в нуль і при
), В якості якого можна розглядати зазначені вище коливання атомів. Ця енергія не залежить від температури, а значить, не звертається в нуль і при 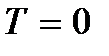 . При низьких температурах класичні уявлення про рух перестають виконуватися. У цій області діють квантові закони, відповідно до яких рух частинок не припиняється, навіть якщо знизити температуру тіла до абсолютного нуля. Але швидкість цього руху вже не залежить від температури і цей рух не є тепловим. Це підтверджується і принципом невизначеності. Якби частки тіла спочивали, то їх положення (координати x, y, Z) і імпульси (проекції імпульсу p x, p y, p z) Були б точно визначені
. При низьких температурах класичні уявлення про рух перестають виконуватися. У цій області діють квантові закони, відповідно до яких рух частинок не припиняється, навіть якщо знизити температуру тіла до абсолютного нуля. Але швидкість цього руху вже не залежить від температури і цей рух не є тепловим. Це підтверджується і принципом невизначеності. Якби частки тіла спочивали, то їх положення (координати x, y, Z) і імпульси (проекції імпульсу p x, p y, p z) Були б точно визначені 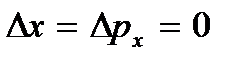 і т.д., а це суперечить співвідношенням невизначеностей
і т.д., а це суперечить співвідношенням невизначеностей 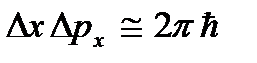 і т.д. Абсолютний нуль не можна досягти. Нижче буде показано, що абсолютний нуль температури означає такий стан системи, при якому система знаходиться в стані з найменшою енергією, і тому подальше зменшення інтенсивності руху її частинок за рахунок віддачі його енергії навколишніх тіл неможливо.
і т.д. Абсолютний нуль не можна досягти. Нижче буде показано, що абсолютний нуль температури означає такий стан системи, при якому система знаходиться в стані з найменшою енергією, і тому подальше зменшення інтенсивності руху її частинок за рахунок віддачі його енергії навколишніх тіл неможливо.Формулу (2.7) можна записати у вигляді.
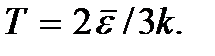
Ця формула може служити визначенням поняття абсолютної температури для одноатомного газу. Температуру будь-який інший системи можна визначити як величину, рівну температурі одноатомного газу, що знаходиться в тепловій рівновазі з цією системою. Визначення температури за допомогою цієї формули вірно аж до температур, при яких вже не можна знехтувати ймовірністю виникнення електронно-збуджених станів атомів газу.
Співвідношення (2.8) дозволяє ввести так звану середню квадратичну швидкість молекули, визначивши її як
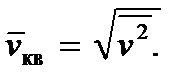
тоді отримаємо
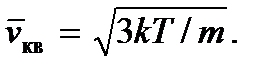
Поняття абсолютної температури можна більш строго ввести в статистичній фізиці, де її можна розглядати як модуль статистичного розподілу часток по енергіях. Відзначимо також, що оскільки температура, так само як і тиск, як видно з формул (2.7) і (2.8), визначається середньої кінетичної енергією молекули ідеального газу, то тони є статистичні величини і, отже, немає сенсу говорити про температуру або тиск одного або невеликого числа молекул.
Вибір в якості основних точок температурної шкали точок танення льоду і кипіння води абсолютно довільний. Отримана таким чином температурна шкалавиявилася незручною для теоретичних досліджень.
Спираючись на закони термодинаміки, Кельвіном вдалося побудувати так звану абсолютну температурну шкалу (її нині називають термодинамічної шкалою температур або шкалою Кельвіна), абсолютно не залежну ні від природи термометрического тіла, ні від обраного термометрического параметра. Однак принцип побудови такої шкали виходить за межі шкільної програми. Ми розглянемо це питання, використовуючи інші міркування.
З формули (2) випливають два можливих способу встановлення температурної шкали: використання зміни тиску певної кількості газу при постійному обсязі або зміна обсягу при постійному тиску. Таку шкалу називають ідеальної газової шкалою температури.
Температура, яка визначається рівністю (2), називається абсолютної температурою. Абсолютна температура? не може бути негативною, так як зліва в рівності (2) стоять свідомо позитивні величини (точніше, вона не може бути різних знаків, вона може бути або позитивною, або негативною. Це залежить від вибору знака постійної k. Так як домовилися температуру потрійної точки вважати позитивною, то абсолютна температура може бути тільки позитивною). Отже, найменше можливе значення температури Т = 0 є температура, коли тиск або обсяг дорівнюють нулю.
Гранична температура, при якій тиск ідеального газу звертається в нуль при фіксованому обсязі або обсяг ідеального газу прагне до нуля (тобто газ як би повинен стиснутися в "точку") при постійному тиску, називається абсолютним нулем. це сама низька температурав природі.
З рівності (3), з огляду на, що
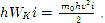
випливає фізичний зміст абсолютного нуля: абсолютний нуль - температура, при якій має припинитися теплове поступальний рух молекул. Абсолютний нуль недосяжний.
У Міжнародній системі одиниць (СІ) використовують абсолютну термодинамічну шкалу температур. За нульову температуру по цій шкалі прийнятий абсолютний нуль. В якості другої опорної точки прийнята температура, при якій знаходяться в динамічній рівновазі вода, лід і насичений пар, так звана потрійна точка (за шкалою Цельсія температура потрійної точки дорівнює 0,01 ° С). Кожна одиниця абсолютної температури, яка називається Кельвіном (позначається 1 К), дорівнює градусу Цельсія.
= .Будь-яке вимірювання припускає наявність точки відліку. Не є винятком і температура. Для шкали Фаренгейта такий нульовою відміткою є температура снігу, змішаного з кухонною сіллю, для шкали Цельсія - температура замерзання води. Але є особлива точка відліку температури - абсолютний нуль.
Абсолютний температурний нуль відповідає 273,15 градусам Цельсія нижче нуля, 459,67 нижче нуля за Фаренгейтом. Для температурної шкали Кельвіна така температура сама по собі є нульовою відміткою.
Сутність абсолютного нуля температури
Поняття абсолютного нуля виходить із самої суті температури. Будь-яке тіло має енергію, яку віддає в навколишнє середовище в ході теплопередачі. При цьому знижується температура тіла, тобто енергії залишається менше. Теоретично цей процес може тривати до тих пір, поки кількість енергії не досягне такого мінімуму, при якому віддавати її тіло вже не зможе.
Віддалене передвістя такої ідеї можна знайти вже у М.В.Ломоносова. Великий російський вчений пояснював теплоту «коловоротні» рухом. Отже, гранична ступінь охолодження - це повна зупинка такого руху.За сучасними уявленнями, абсолютний нуль температури - це такий стан речовини, при якому молекули найменшим можливим рівнем енергії. При меншій кількості енергії, тобто при більш низькій температурі жодне фізичне тіло існувати не може.
Теорія та практика
Абсолютний нуль температури - поняття теоретичне, досягти його на практиці неможливо в принципі, навіть в умовах наукових лабораторій з найскладнішою апаратурою. Але вченим вдається охолоджувати речовина до дуже низьких температур, які близькі до абсолютного нуля.
При таких температурах речовини набувають дивовижні властивості, яких вони не можуть мати при звичайних обставинах. Ртуть, яку називають «живим сріблом» через її перебування в стані, близькому до рідкого, при такій температурі стає твердою - до такої міри, що нею можна забивати цвяхи. Деякі метали стають крихкими, як скло. Такий же твердої і крихкої стає гума. Якщо при температурі, близькій до абсолютного нуля, вдарити молотком який-небудь гумовий предмет, він розіб'ється, як скляний.
Така зміна властивостей теж пов'язано з природою теплоти. Чим вище температура фізичного тіла, тим інтенсивніше і хаотичнее рухаються молекули. У міру зниження температури рух стає менш інтенсивним, а структура - більш упорядкованим. Так газ стає рідиною, а рідина твердим тілом. Граничний рівень впорядкованості - кристалічна структура. При наднизьких температурах її набувають навіть такі речовини, які в звичайному стані залишаються аморфними, наприклад, гума.
Цікаві явища відбуваються і з металами. Атоми кристалічної решітки коливаються з менше амплітудою, розсіювання електронів зменшується, тому падає електричний опір. Метал набуває надпровідність, практичне застосування якої є досить привабливим, хоча і важкодосяжним.
Граничну температуру, при якій обсяг ідеального газу стає рівним нулю, приймають за абсолютний нуль температури. Однак обсяг реальних газів при абсолютному нулі температури звертатися в нуль не може. Чи має сенс тоді це граничне значення температури?
Гранична температура, існування якої випливає з закону Гей-Люссака, має сенс, тому що практично можна наблизити властивості реального газу до властивостей ідеального. Для цього треба брати все більш розріджене газ, так щоб його щільність наближалася до нуля. У такого газу дійсно обсяг зі зниженням температури буде прагнути до граничного, близькому до нуля.
Знайдемо значення абсолютного нуля за шкалою Цельсія. прирівнюючи обсяг Vвформулою (3.6.4) нулю і з огляду на, що
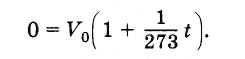
Звідси абсолютний нуль температури дорівнює
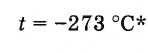
* Більш точне значення абсолютного нуля: -273,15 ° С.
Це гранична, найнижча температура в природі, та «найбільша або остання ступінь холоду», існування якої передбачив Ломоносов.
шкала Кельвіна

Кельвін Вільям (Томсон У.) (1824 1907) - видатний англійський фізик, один із засновників термодинаміки і молекулярно-кінетичної теорії газів.
Кельвін ввів абсолютну шкалу температур і дав одне з формулювань другого початку термодинаміки у формі неможливості повного перетворення теплоти в роботу. Він зробив розрахунок розмірів молекул на основі вимірювання поверхневої енергії рідини. У зв'язку з прокладанням трансатлантичного телеграфного кабелю Кельвін розробив теорію електромагнітних коливань і вивів формулу для періоду вільних коливань в контурі. За наукові заслуги У. Томсон отримав титул лорда Кельвіна.
Англійський учений У. Кельвін ввів абсолютну шкалу температур. Нульова температура за шкалою Кельвіна відповідає абсолютного нуля, і одиниця температури по цій шкалі дорівнює градусу за шкалою Цельсія, тому абсолютна температура Тпов'язана з температурою за шкалою Цельсія формулою
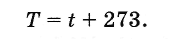 (3.7.6)
(3.7.6)На малюнку 3.11 для порівняння зображені абсолютна шкала і шкала Цельсія.
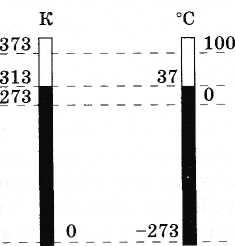
Одиниця абсолютної температури в СІ називається Кельвіном (скорочено К). Отже, один градус за шкалою Цельсія дорівнює одному градусу за шкалою Кельвіна: 1 ° С = 1 К.
Таким чином, абсолютна температура за визначенням, що дається формулою (3.7.6), є похідною величиною, що залежить від температури за Цельсієм і від експериментально визначається значення а. Однак вона має фундаментальне значення.
З точки зору молекулярно-кінетичної теорії абсолютна температура пов'язана з середньою кінетичної енергією хаотичного руху атомів або молекул. при Т =Про До тепловий рух молекул припиняється. Детальніше про це піде мова в розділі 4.
Залежність обсягу від абсолютної температури
Застосовуючи шкалу Кельвіна, закон Гей-Люссака (3.6.4) можна записати в більш простій формі. Так як
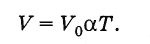 (3.7.7)
(3.7.7)Обсяг газу даної маси при постійному тиску прямо пропорційний абсолютній температурі.
Звідси випливає, що відношення обсягів газу однієї і тієї ж маси в різних станах при одному і тому ж тиску дорівнює відношенню абсолютних температур:
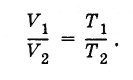 (3.7.8)
(3.7.8)Існує мінімально можлива температура, при якій обсяг (і тиск) ідеального газу звертаються в нуль. Це абсолютний нуль температури:-273 ° С. Зручно відраховувати температуру від абсолютного нуля. Так будується абсолютна шкала температур.