Az a tény, hogy minden izobár egy ponton konvergál (1.9. ábra), nem véletlen, hanem egy bizonyos mintázat. fizikai jelentése. Meleg-Lussac törvénye nem tagadja a korlátlan hőmérséklet-növekedés lehetőségét, mert a növekvő hőmérséklet mellett a gáz térfogata korlátlanul növekedhet. Ennek ellenére a hőmérséklet csökkenésével nullára hajlik, és van egy határértéke ( V=0), mivel nem lehet negatív.
Valójában a valódi gázok még ezt a határt sem érhetik el, mivel atomjaik és molekuláik, bár kicsik, mégis rendelkeznek bizonyos térfogattal.
Ha az Eq. (V-V 0) /V 0 =αΔ t, azt feltételezni V 0 — a gáz térfogata at t 0= 0°C tehát Δ t =t-t 0 =t,és egyenlővé tesszük nullával, mint a térfogat alsó határával, akkor megkapjuk a Celsius-skála legalacsonyabb hőmérsékletének értékét, amellyel a testek rendelkezhetnek:
0 = V 0. (1 + t / 273).
1 + t / 273 = 0, t = -273°C
Tehát a hőmérséklet korlátlanul emelkedhet, de a természetben megvan az alsó határ - abszolút nulla, ami alá nem eshet. Ez az oka annak, hogy az összes gáz izobárjai a hőmérsékleti tengely egy pontjában konvergálnak, ami -273°C.
A világon nem minden relatív; Vannak abszolút értékek is, különösen abszolút nulla hőmérséklet.
Létezés abszolút nulla hőmérséklet W. Thomson angol tudós alapította. Kelvin) az építkezés alapjaként abszolút hőmérsékleti skála, amely nem függ a metrikus test tulajdonságaitól, ezért ideálisnak tekinthető. Anyag az oldalról

William Thomson (Lord Kelvin) (1824 - 1907). Angol fizikus, a termodinamika és a molekuláris kinetikai elmélet, a termoelektromos jelenségek elméletének, az elektromágneses rezgések alapjainak egyik megalapozója. Megfogalmazta a termodinamika második főtételét, bevezette az abszolút hőmérsékleti skálát (Kelvin-skála), felfedezte a termodinamikai hatást, levezette a természetes elektromágneses rezgések periódusának képletét oszcillációs körben, számításokat végzett a molekulák méretére, stb. tudományos eredményeket megkapta a Lord Kelvin címet.
A skála kiindulópontja az abszolút nulla hőmérséklet, melynek pontos értéke -273,15° C. A választott mértékegység az az érték, amelyet SI-ben hívunk. Kelvin(TO); akkora, mint egy fok Celsius(°C): 1 K = 1 °C. Ezért az abszolút hőmérséklet között Tés a hőmérséklet Celsius-skálán t egyszerű összefüggés van (1.10. ábra):
T=t + 273.
Koncepció abszolút hőmérséklet széles körben használják a termodinamikában és a molekuláris fizikában, mivel mély fizikai jelentéssel bír, és számos egyenlet felírását leegyszerűsíti.
Ezen az oldalon a következő témákban található anyagok:
Termodinamikai hőmérséklet skála abszolút nulla absztrakt
Előadás abszolút hőmérsékleti skála
Hőelektromos jelenségek és molekuláris fizika
-
A hőmérséklet a test „melegének” mennyiségi mértéke. A hőmérséklet fogalma különleges helyet foglal el között fizikai mennyiségek, amely meghatározza a rendszer állapotát. A hőmérséklet nem csak egy adott test termikus egyensúlyi állapotát jellemzi. Ez az a paraméter is, amely ugyanazt az értéket veszi fel bármely két vagy több egymással termikus egyensúlyban lévő testre, pl. testrendszer termikus egyensúlyát jellemzi. Ez azt jelenti, hogy ha két vagy több különböző hőmérsékletű test érintkezik, akkor a molekulák közötti kölcsönhatás eredményeként ezek a testek azonos hőmérsékleti értéket vesznek fel.
A molekuláris kinetikai elmélet lehetővé teszi a hőmérséklet fizikai jelentésének tisztázását. A (2.4) és (2.7) kifejezéseket összehasonlítva azt látjuk, hogy egybeesnek, ha feltesszük
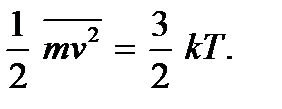 (2.9)
(2.9)Ezeket az összefüggéseket a gázok molekuláris kinetikai elméletének második alapegyenleteinek nevezzük. Azt mutatják abszolút hőmérséklet olyan mennyiség, amely meghatározza a molekulák transzlációs mozgásának átlagos kinetikus energiáját; ez a molekulák transzlációs mozgásának energiájának, és ezáltal a molekulák hőmozgásának intenzitásának mértéke. Ez az abszolút hőmérséklet molekuláris kinetikai jelentése. Amint látjuk, a test felmelegedésének folyamata közvetlenül kapcsolódik a test részecskéinek átlagos kinetikus energiájának növekedéséhez. A (2.9)-ből világos, hogy az abszolút hőmérséklet pozitív mennyiség:
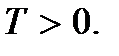 Jelentése
Jelentése 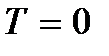 abszolút nulla hőmérsékletnek nevezzük. A (2.8) szerint abszolút nullánál a részecskék transzlációs mozgásának teljesen le kell állnia (
abszolút nulla hőmérsékletnek nevezzük. A (2.8) szerint abszolút nullánál a részecskék transzlációs mozgásának teljesen le kell állnia ( 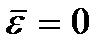 ). Meg kell azonban jegyezni, hogy alacsony hőmérsékleten a gáz lecsapódik. Következésképpen minden, a gázok kinetikai elmélete alapján levont következtetés értelmét veszti. És abszolút nulla hőmérsékleten a mozgás nem tűnik el. Az elektronok mozgása az atomokban és a szabad elektronok mozgása a fémekben még abszolút nulla hőmérsékleten is teljesen megmarad. Ezen túlmenően, még abszolút nullánál is megmarad az atomok rezgésmozgása a molekulákon belül és a kristályrács csomópontjain lévő atomok. Ezeknek a rezgéseknek a létezése a kvantumharmonikus oszcillátorban lévő nullponti energia jelenlétével függ össze (
). Meg kell azonban jegyezni, hogy alacsony hőmérsékleten a gáz lecsapódik. Következésképpen minden, a gázok kinetikai elmélete alapján levont következtetés értelmét veszti. És abszolút nulla hőmérsékleten a mozgás nem tűnik el. Az elektronok mozgása az atomokban és a szabad elektronok mozgása a fémekben még abszolút nulla hőmérsékleten is teljesen megmarad. Ezen túlmenően, még abszolút nullánál is megmarad az atomok rezgésmozgása a molekulákon belül és a kristályrács csomópontjain lévő atomok. Ezeknek a rezgéseknek a létezése a kvantumharmonikus oszcillátorban lévő nullponti energia jelenlétével függ össze ( 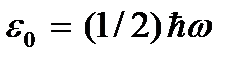 ), amelyek az atomok fenti rezgéseinek tekinthetők. Ez az energia nem függ a hőmérséklettől, ami azt jelenti, hogy még a hőmérséklettől sem tűnik el
), amelyek az atomok fenti rezgéseinek tekinthetők. Ez az energia nem függ a hőmérséklettől, ami azt jelenti, hogy még a hőmérséklettől sem tűnik el 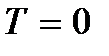 . Alacsony hőmérsékleten a mozgásról szóló klasszikus elképzelések már nem igazak. Ezen a területen kvantumtörvények működnek, amelyek szerint a részecskék mozgása akkor sem áll le, ha a test hőmérsékletét abszolút nullára csökkentjük. De ennek a mozgásnak a sebessége már nem függ a hőmérséklettől, és ez a mozgás nem termikus. Ezt erősíti meg a bizonytalanság elve. Ha a test részecskéi nyugalomban voltak, akkor helyzetük (koordináta x, y, z) és impulzusok (impulzusvetületek p x, p y, p z) lenne pontosan meghatározva
. Alacsony hőmérsékleten a mozgásról szóló klasszikus elképzelések már nem igazak. Ezen a területen kvantumtörvények működnek, amelyek szerint a részecskék mozgása akkor sem áll le, ha a test hőmérsékletét abszolút nullára csökkentjük. De ennek a mozgásnak a sebessége már nem függ a hőmérséklettől, és ez a mozgás nem termikus. Ezt erősíti meg a bizonytalanság elve. Ha a test részecskéi nyugalomban voltak, akkor helyzetük (koordináta x, y, z) és impulzusok (impulzusvetületek p x, p y, p z) lenne pontosan meghatározva 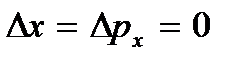 stb., és ez ellentmond a bizonytalansági viszonyoknak
stb., és ez ellentmond a bizonytalansági viszonyoknak 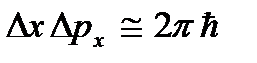 stb. Az abszolút nulla nem elérhető. Az alábbiakban bemutatjuk, hogy az abszolút nulla hőmérséklet a rendszernek azt az állapotát jelenti, amelyben a rendszer a legalacsonyabb energiájú állapotban van, és ezért a részecskéi mozgásának intenzitása tovább csökken az energiájának átadása miatt. környező testek nem lehetséges.
stb. Az abszolút nulla nem elérhető. Az alábbiakban bemutatjuk, hogy az abszolút nulla hőmérséklet a rendszernek azt az állapotát jelenti, amelyben a rendszer a legalacsonyabb energiájú állapotban van, és ezért a részecskéi mozgásának intenzitása tovább csökken az energiájának átadása miatt. környező testek nem lehetséges.A (2.7) képlet a formába írható.
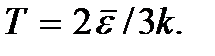
Ez a képlet egy monoatomos gáz abszolút hőmérséklete fogalmának definíciójaként szolgálhat. Bármely más rendszer hőmérséklete meghatározható az ezzel a rendszerrel termikus egyensúlyban lévő egyatomos gáz hőmérsékletével megegyező értékként. A hőmérséklet meghatározása ezzel a képlettel egészen olyan hőmérsékletig helyes, amelynél a gázatomok elektronikusan gerjesztett állapotának bekövetkezésének valószínűsége már nem elhanyagolható.
A (2.8) reláció lehetővé teszi, hogy bemutassuk egy molekula úgynevezett négyzetes középsebességét, definiálva azt
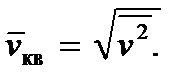
Akkor kapunk
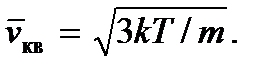
Az abszolút hőmérséklet fogalma szigorúbban bevezethető a statisztikus fizikába, ahol a részecskék energia szerinti statisztikai eloszlásának modulusának tekinthető. Vegye figyelembe azt is, hogy mivel a hőmérsékletet, akárcsak a nyomást, amint az a (2.7) és (2.8) képletekből látható, egy ideális gázmolekula átlagos kinetikus energiája határozza meg, ezért statisztikai mennyiségeket képviselnek, ezért nincs értelme beszélni egy vagy kis számú molekula hőmérsékletéről vagy nyomásáról.
A jégolvadás és a forrásban lévő víz pontjainak megválasztása a hőmérsékleti skála fő pontjaként teljesen önkényes. Így szerezték be hőmérsékleti skála az elméleti kutatás szempontjából kényelmetlennek bizonyult.
A termodinamika törvényei alapján Kelvinnek sikerült megszerkesztenie az úgynevezett abszolút hőmérsékleti skálát (jelenleg termodinamikai hőmérsékleti skálának vagy Kelvin-skálának hívják), teljesen függetlenül akár a hőmérő test természetétől, akár a kiválasztott hőmérős paramétertől. Az ilyen skála felépítésének elve azonban túlmutat az iskolai tananyagon. Ezt a kérdést más szempontok alapján fogjuk megvizsgálni.
A (2) képlet két lehetséges módot tartalmaz a hőmérsékleti skála létrehozására: egy bizonyos mennyiségű gáz nyomásának változását állandó térfogat mellett, vagy a térfogat változtatását állandó nyomás. Ezt a skálát ún ideális gázhőmérséklet skála.
A (2) egyenlőséggel meghatározott hőmérsékletet ún abszolút hőmérséklet. Abszolút hőmérséklet? nem lehet negatív, mivel a (2) egyenlőség bal oldalán nyilvánvalóan pozitív mennyiségek vannak (pontosabban nem lehet különböző előjelű; lehet pozitív vagy negatív. Ez a k konstans előjelének megválasztásától függ. Mivel a hármaspont hőmérsékletét pozitívnak tekintjük, ezért az abszolút hőmérséklet csak pozitív lehet). Ezért a lehető legalacsonyabb hőmérsékleti érték T = 0 az a hőmérséklet, amikor a nyomás vagy a térfogat nulla.
Azt a határhőmérsékletet, amelynél az ideális gáz nyomása meghatározott térfogaton eltűnik, vagy az ideális gáz térfogata nullára hajlik (vagyis a gázt egy „pontba” kell sűríteni) állandó nyomáson ún. abszolút nulla. Ez a legtöbb alacsony hőmérséklet a természetben.
Az egyenlőségből (3), figyelembe véve azt
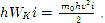
Az abszolút nulla fizikai jelentése a következő: az abszolút nulla az a hőmérséklet, amelyen a molekulák termikus transzlációs mozgásának meg kell szűnnie. Az abszolút nulla elérhetetlen.
A Nemzetközi Mértékegységrendszer (SI) abszolút termodinamikai hőmérsékleti skálát használ. Ezen a skálán az abszolút nulla nulla hőmérsékletnek számít. A második referenciapont az a hőmérséklet, amelyen a víz, a jég és a telített gőz dinamikus egyensúlyban van, az úgynevezett hármaspont (a Celsius-skálán a hármaspont hőmérséklete 0,01 °C). Az abszolút hőmérséklet minden egysége, amelyet Kelvinnek neveznek (jelképez 1 K), egyenlő egy Celsius-fokkal.
= .Minden méréshez referenciapont megléte szükséges. A hőmérséklet sem kivétel. A Fahrenheit-skála esetében ez a nullapont a konyhasóval kevert hó hőmérséklete, a Celsius-skála esetében a víz fagyáspontja. De van egy speciális hőmérsékleti referenciapont - abszolút nulla.
A nulla abszolút hőmérséklet 273,15 Celsius-fok nulla alatt, 459,67 0 Fahrenheit alatti. A Kelvin hőmérsékleti skála esetében ez a hőmérséklet maga a nulla jel.
Az abszolút nulla hőmérséklet lényege
Az abszolút nulla fogalma a hőmérséklet lényegéből ered. Bármely test rendelkezik energiával, amelyet a hőátadás során a külső környezetbe bocsát ki. Ezzel párhuzamosan csökken a testhőmérséklet, i.e. kevesebb energia marad. Elméletileg ez a folyamat addig folytatódhat, amíg az energia mennyisége el nem éri azt a minimumot, hogy a szervezet már nem tudja leadni.
Egy ilyen ötlet távoli hírnöke már megtalálható M. V. Lomonoszovban. A nagy orosz tudós a hőt „forgó” mozgással magyarázta. Következésképpen a maximális hűtési fokozat az ilyen mozgás teljes leállítását jelenti.A modern fogalmak szerint az abszolút nulla hőmérséklet olyan halmazállapot, amelyben a molekulák a lehető legalacsonyabb energiaszinttel rendelkeznek. Kevesebb energiával, pl. alacsonyabb hőmérsékleten nem létezhet fizikai test.
Elmélet és gyakorlat
Az abszolút nulla hőmérséklet elméleti koncepció, a gyakorlatban még a legkifinomultabb berendezésekkel rendelkező tudományos laboratóriumokban sem lehet elérni. De a tudósoknak sikerül lehűteni az anyagot nagyon alacsony hőmérsékletre, amely közel van az abszolút nullához.
Ilyen hőmérsékleten az anyagok olyan elképesztő tulajdonságokra tesznek szert, amelyekkel rendes körülmények között nem rendelkezhetnek. A higany, amelyet "élő ezüstnek" neveznek, mivel a folyadékhoz közeli állapotban van, ezen a hőmérsékleten megszilárdul - olyan mértékben, hogy szögek beverésére is használható. Egyes fémek törékennyé válnak, például az üveg. A gumi ugyanolyan kemény és törékennyé válik. Ha az abszolút nullához közeli hőmérsékleten kalapáccsal megüt egy gumitárgyat, az üvegszerűen törik.
Ez a tulajdonságváltozás a hő természetével is összefügg. Minél magasabb a fizikai test hőmérséklete, annál intenzívebben és kaotikusabban mozognak a molekulák. A hőmérséklet csökkenésével a mozgás kevésbé intenzív, a szerkezet rendezettebbé válik. Tehát a gázból folyékony, a folyadékból szilárd halmazállapotú lesz. A rendezettség végső szintje a kristályszerkezet. Ultra-alacsony hőmérsékleten még az általában amorf anyagok, például a gumi is felveszik azt.
Érdekes jelenségek a fémekkel is előfordulnak. A kristályrács atomjai kisebb amplitúdóval rezegnek, csökken az elektronszórás, ezért csökken az elektromos ellenállás. A fém szupravezetésre tesz szert, aminek gyakorlati alkalmazása igen csábítónak tűnik, bár nehezen megvalósítható.
Abszolút nulla hőmérsékletnek azt a határhőmérsékletet vesszük, amelyen az ideális gáz térfogata nullával egyenlővé válik. A valódi gázok térfogata azonban abszolút nulla hőmérsékleten nem tűnhet el. Akkor ennek a hőmérsékleti határnak van értelme?
A határhőmérséklet, amelynek megléte a Gay-Lussac törvényből következik, logikus, hiszen gyakorlatilag lehetséges egy valódi gáz tulajdonságait az ideálishoz közelíteni. Ehhez egyre ritkább gázt kell venni, hogy a sűrűsége nullára csökkenjen. Valójában a hőmérséklet csökkenésével az ilyen gáz térfogata a határértékre, a nullához közeli lesz.
Keressük meg az abszolút nulla értékét a Celsius-skálán. Hangerő egyenlővé tétele VV(3.6.4) képlet nulla, és ezt figyelembe véve
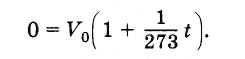
Ezért az abszolút nulla hőmérséklet az
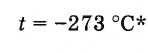
* Pontosabb abszolút nulla érték: -273,15 °C.
Ez a természet szélsőséges, legalacsonyabb hőmérséklete, a „legnagyobb vagy utolsó hidegfok”, amelynek létezését Lomonoszov megjósolta.
Kelvin skála

Kelvin William (Thomson W.) (1824-1907) - kiváló angol fizikus, a termodinamika és a gázok molekuláris kinetikai elméletének egyik megalapítója.
Kelvin bevezette az abszolút hőmérsékleti skálát, és megadta a termodinamika második főtételének egyik megfogalmazását a hő teljes munkává alakításának lehetetlenségében. A folyadék felületi energiájának mérése alapján számította ki a molekulák méretét. A transzatlanti távírókábel lefektetésével kapcsolatban Kelvin kidolgozta az elektromágneses rezgések elméletét, és levezette az áramkör szabad rezgésének periódusának képletét. Tudományos eredményeiért W. Thomson Lord Kelvin címet kapott.
W. Kelvin angol tudós bemutatta az abszolút hőmérsékleti skálát. A Kelvin-skála nulla hőmérséklete az abszolút nullának felel meg, a hőmérséklet mértékegysége pedig a Celsius-skála egy fokkal, tehát abszolút hőmérséklet T képlettel viszonyul a Celsius-skála hőmérsékletéhez
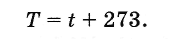 (3.7.6)
(3.7.6)A 3.11. ábra az abszolút skálát és a Celsius-skálát mutatja összehasonlítás céljából.
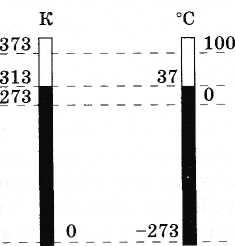
Az abszolút hőmérséklet SI mértékegységét kelvinnek (rövidítve K) nevezzük. Ezért a Celsius-skála egy foka egyenlő a Kelvin-skála egy fokával: 1 °C = 1 K.
Így az abszolút hőmérséklet a (3.7.6) képlet definíciója szerint olyan származtatott mennyiség, amely a Celsius-hőmérséklettől és a kísérletileg meghatározott értékétől függ. Ennek azonban alapvető jelentősége van.
A molekuláris kinetikai elmélet szempontjából az abszolút hőmérséklet az atomok vagy molekulák kaotikus mozgásának átlagos kinetikai energiájához kapcsolódik. at T = O K a molekulák hőmozgása leáll. Erről részletesebben a 4. fejezetben lesz szó.
A térfogat függése az abszolút hőmérséklettől
A Kelvin-skála segítségével a Gay-Lussac-törvény (3.6.4) egyszerűbb formában is felírható. Mert
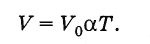 (3.7.7)
(3.7.7)Egy adott tömegű gáz térfogata állandó nyomáson egyenesen arányos az abszolút hőmérséklettel.
Ebből következik, hogy az azonos tömegű gáz térfogatának aránya különböző állapotokban, azonos nyomáson megegyezik az abszolút hőmérsékletek arányával:
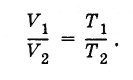 (3.7.8)
(3.7.8)Van egy minimális lehetséges hőmérséklet, amelynél az ideális gáz térfogata (és nyomása) eltűnik. Ez abszolút nulla hőmérséklet:-273 °C. Kényelmes a hőmérsékletet abszolút nullától számítani. Így épül fel az abszolút hőmérsékleti skála.